ニュースでアメリカの有名人が線維性筋痛症で芸能活動休止すると報告して話題になりました。日本でも線維性筋痛症が原因での不幸な報道が昔からあります。身体の疼くような痛み、こわばり、とても酷い疲労感、痺れなどが局所的、全身的にあり慢性的で睡眠障害や抑うつ状態なども併発します。痛みは、とても酷く耐え難い状態が多くみられます。身体を動かすと痛みが大きくなります。症状が悪化すると安静にしていても痛み続けます。医学的には原因は不明で脳に原因を求める文献が多いのが特徴です。
カイロプラクティックは、線維性筋痛症においてもっとも有効な治療のひとつとされ、それ以外の手段は休息のみです。*1 当院でも臨床上は高い改善があり、部分的な症状だとその場で症状消失することが多いです。
個人的な見解を述べると、腰痛治療と同じく身体(筋肉)への関節や筋肉の負荷を取り除くとほとんどのケースで改善します。痛みが異常に大きい事が従来の筋骨格症状と違いますが、痛みを感じる脳の部分の過剰反応とその反応の抑制が働いてない事など考えられます。
そういった脳の問題もあるとは思いますが、末梢(筋肉の負担)を改善するのが現在の線維性筋痛症の治療では現実的だと思います。
以後、各論に続きます。
原因
原因は不明です。リウマチ性疾患に分類されてるようですが、リウマチ血液検査でリウマチ因子(RF)は陰性です。症状がリウマチに似ているというだけの分類でしたら意味はありません。この分類は、医師の症状への混乱が見て取れます。
ちなみに腰痛も原因が不明です。ここで腰痛で来院され簡単に改善された方は、筋骨格の機能が原因でまたお医者さん達は分からないと言っているのではないかと勘ぐられると思います。当院の臨床的にはその通りです。
しかし、下行性痛覚制御経路の問題(痛みの抑制が働いてない)も含んでいる可能性があります。その様に中枢性の問題が絡んでる様な特異な症状なので、腰痛治療の様に簡単ではありません。長期に渡って悪化している場合は触診するのも難しい場合もあります。
症状
全身の疼痛を主症状として不眠、うつ病、胃腸や内臓の自律神経系症状を伴うことがあります。近年は粘膜系の障害が高頻度で伴うということです。激しい痛みが全身に拡散します。
40代から50代が多くいわゆる働き盛りの女性に多い事が特徴です。全国200万人以上の患者がいて、その80%を女性が占めてます。*2
一般人はもとより医師、医療従事者に正しい情報が著しく欠落してます。有名人報道によって症状の理解が深まるのは良い事です。
診断法
smytheが1980年に考案した基準があります。3)
- 主観的な疼痛が3か月以上続いている。
- こわばりも3か月以上続いてる。
- 複数の部位に圧痛点がある。
- 血液検査、画像診断所見が正常で、リウマチ因子もでない。
1-4までは必ず該当しなくてはなりません。
代表的な診断基準としては米国リウマチ学会が1990年に作成しました。身体に18か所の圧痛点がある基準というものです(図1)。
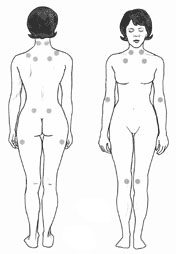
(図1)
しかし、圧痛点は症状の進行度合いによって変化するもので絶対的なものではありません。2010年に同学会は患者自身が症状を主観的にとらえてそれぞれの症状ポイントを加算して評価する方式を作成しました。
これらは日本の医師によっておこなわれてるのかは疑問です。なぜなら、臨床検査で陽性がでない診断はかなりいい加減なので。
当院では、線維性筋痛症様の症状の方がいらっしゃると、病院での診断を受けて貰います。smytheの基準4番(血液検査、画像診断所見が正常で、リウマチ因子もでない。)が該当するかとても重要です。リウマチはカイロプラクティックでは禁忌です。
リウマチ性疾患について簡単に触れておきます。関節リウマチ、手指の関節が左右対称的に腫脹することが多いです。シェーグレン症候群、口腔乾燥と眼球乾燥が多く、線維性筋痛症でも併発している症状で二番目に多い粘膜系の障害です。強直性脊椎炎や多発性、皮膚筋炎などがあります。これらは病院で鑑別されます。
トリガーポイントについて
線維性筋痛症の評価の基準は、smytheも米国リウマチ学会も身体にできた圧痛点を使用してます。その圧痛点とはトリガーポイントと言います。日本語で硬結と言います。そのトリガーポイントについてみていきたいと思います。
トリガーポイントは、筋腹や腱にできる小結節(小さなしこりの様)です。容易に触診可能です。トリガーポイントを圧迫すると軽い不快感からとても激しい痛みまで範囲が広く、酷い場合は、耐え難いと表現する事もあります。「ジャンプ徴候」といって筋痙攣を起こし無意識で反射的な動きをするほどです。*
4
遠く離れた部位に痛みや痺れを広く放散します。その放散痛はそれぞれの筋肉によりパターン化され再現性があります。線維性筋痛症との放散痛パターンとは異なってます。中枢神経系の問題が大きくなると放散パターンが違ってくるのは推測できます。
性別の罹患率では、線維性筋痛症と同じく、女性の方が罹患しやすいと*5
データーがでてます。
以前の症例でトリガーポイントについて触れてますので参考までにお読みください。
https://chiro-matsuyama.ehime.jp/case-foot-numbness/ (太腿裏の痺れ)
https://chiro-matsuyama.ehime.jp/case-herniateddisk3/(腰椎椎間板ヘルニア)
まとめ
線維性筋痛症は、トリガーポイントが全身に多数存在し自律神経症状とペインスパイラルを形成して悪循環化してると考えられます。もし、中枢系の問題だとしても、現時点では対処方法がないので、末梢の筋肉から負担を減らすのが現実的です。高次脳機能障害の場合も末梢の筋肉からの刺激で脳が賦活するのはよく知られてます。
最後に
筋膜痛は深刻に考える必要はないと思うのは、誤ってます。アメリカの有名歌手も休暇をよぎなくされ、水泳選手もトリガーポイントの筋肉痙攣によって溺れる事があります。非常に多くの人が苦しんでます。身体で最大の質量をもつ組織である筋肉を病態生理学上軽視され過ぎであることに懸念を感じます。
筋膜痛は、睡眠障害や不安感など精神的な問題を伴い、お互いの症状が悪い影響を与え合い悪化、永続化する場合があります。そうならないために早めの改善を当院でおこなってください。
<参考文献>
- Wolfe f: The clinical syndrome of fibrositis. Am j Med 81:81, 1986
- 線維筋痛症診療ガイドライン2013 日本線維筋痛症学会編 https://minds.jcqhc.or.jp/docs/minds/FMS/CPGs2017_FM.pdf(最終検索日:2023年5月21日)
- smythe HA: Fibrositis and other diffuse musculoskeletal syndromes. In Kelley WH, Havis JR, Ruddy S, et al.(eds):Textbook of Rheumatology. Philadelphia, WB Saunders, 1980, p485-493
- Good MG: Acroparaesthesia-an idiopathicmyalgia of elbow. Edinburgh Med/ 56:366-368, 1949
- Butler JH Folke LEA, Bandt CL: A descriptive survey of signs and symptoms associated with the myofascial pain-dysfunction syndrome. J Am Dent Assoc 90:635-639, 1975
